对于细胞治疗产品的全生命周期我们也可以按照传统小分子药物一样分为四个阶段,从研发、到技术转移、再到商业化生产、再到产品退市。这是细胞治疗药物的一个生命周期,在整个生命周期中,不同的阶段都会涉及到不同的质量控制策略,例如工艺的管理、质量体系的建设、质量风险管理等,总之我们要有一个系统的科学理解产品知识,贯彻于产品的全生命周期中。
从产品验证的生命周期来讲,可以分为三个阶段,工艺设计、工艺确认、持续工艺验证,如下图所示。
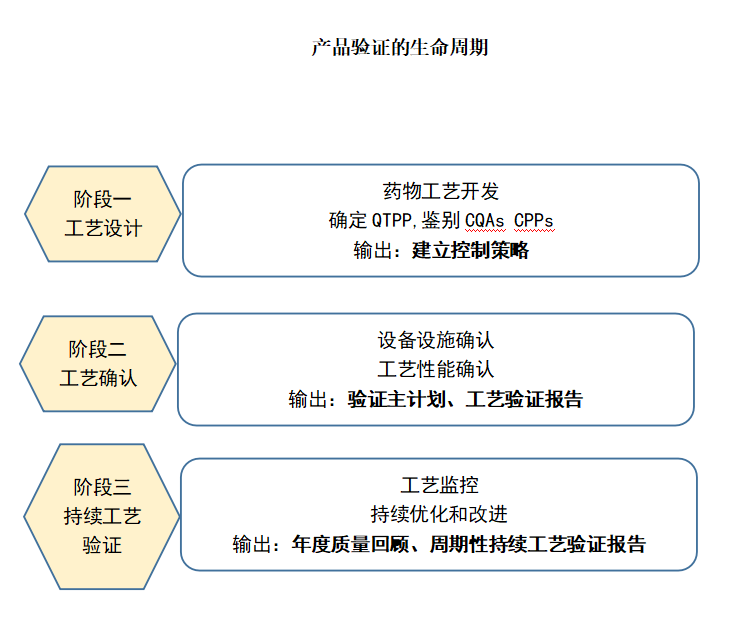
从产品验证的生命周期来说,建立控制策略、制定验证主计划、工艺验证报告、年度回顾、周期性持续性工艺验证报告,组成了质量管理体系。
工艺验证阶段的质控对象
在工艺验证阶段,建立控制策略是最重要的一点,从以下四个方面分析:
首先,核心外围是对工艺的理解。对于工艺参数的控制,基于我们对产品的理解,因此,要对产品深入分析,并在这基础上加以控制。
其次,是对物料属性的控制。起始物料,比如血细胞及其它来源的细胞;其它来源的原材料,用到的培养基和耗材,对于这些物料属性的控制也是非常重要的,它会直接或间接影响产品的关键质量属性。
再者,是对操作的控制。特别是对于操作规程的有效执行,主要涉及到人员、设备、设施及无菌操作等。
最后,是对质量检测的控制。包括工艺过程中的工艺表征研究、中控数据,直至终产品的检验数据。
制订全生命周期的控制策略
在工艺设计阶段,建立控制策略过程中,会用到很多风险评估工具,评估产品关键质量属性,关键工艺参数和物料属性,评估工艺能力,最终确定工艺操作范围。因此,要从产品的全生命周期出发,建立整体的质量控制策略,有助于我们了解产品相关监管的法规要求,同时全生命周期控制策略更加关注工艺开发、工艺表征和工艺的稳定性,了解原材料对产品质量的影响,了解关键工艺步骤和体系,再建立商业化验证策略。
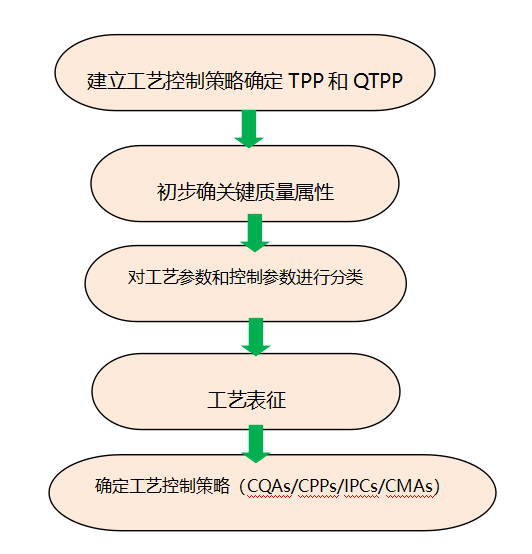
对于细胞治疗产品来说,要在早期关注产品的质量属性,这样对于后期的工艺开发及放大是非常重要的。细胞治疗产品的特殊性,无论从作用机制、产品本身的变异性、临床开发的策略、产品本身半衰期比较短的特点(货架期短、稳定性差),还是其产能扩大不同传统的倍数放大逻辑而言,加之细胞治疗相关的法律法规及指导原则都在不断的更新优化,这些都是挑战,也是要求从产品的全生命周期去开发细胞治疗生产工艺,建立工艺控制策略。
细胞治疗产品的挑战:
生物药不同于小分子药物遇到的挑战,这种挑战表现在更多方面。
快速临床试验发展和工艺变化,推动了对工艺和产品的理解,需要在此基础上去做对比研究和开发控制策略。
同时,工艺开发也需要多职能团队参与其中,如工艺和分析方法开发人员,生产人员、质量管理人员、注册人员、临床试验等。
因此,细胞治疗药物在产品开发阶段就建议使用全生命周期的质量控制策略,有效利用产品开发各阶段的关键数据,为CMC决策提供帮助,通过了解产品的质量属性,将关键质量属性与关键工艺参数联系起来,建立稳定的一致性的生产工艺。
(来源:蒲公英)